"नाइट्रेट" के अवतरणों में अंतर
imported>Samyak005 (xmlpage created) |
imported>रोहित साव27 (+छवि #WPWP #WPWPHI) |
||
| पंक्ति १: | पंक्ति १: | ||
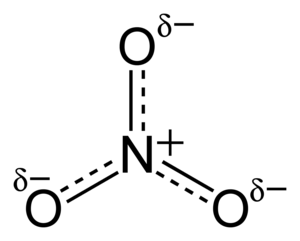
[[File:Nitrate-ion-with-partial-charges-2D.png|thumb|दिखाए गए आंशिक आरोपों के साथ नाइट्रेट आयन]] | |||
'''नाइट्रेट''' (nitrate) [[कार्बन|कार्बन [carbon]]<nowiki>] और </nowiki>[[नाइट्रोजन]] [[रासायनिक तत्व|तत्वों]] [nitrogen] का बना एक [[आयन#ऋणायन और धनायन|ऋणायन]] (निगेटिव आवेश वाला [[आयन]]) होता है। इसका [[रासायनिक सूत्र]] NO<sub>3</sub><sup>−</sup> है। यह [[अमोनियम नाइट्रेट]] जैसे कई [[रासायनिक यौगिक]]ों (कम्पाउंड) का अंश है।<ref>Wolfgang Laue, Michael Thiemann, Erich Scheibler, Karl Wilhelm Wiegand "Nitrates and Nitrites" in Ullmann's Encyclopedia of Industrial Chemistry, 2006, Wiley-VCH, Weinheim. doi:10.1002/14356007.a17_265</ref> | |||
[[धातु|धातुओं]] अथवा उनके ऑक्साइड पर [[नाइट्रिक अम्ल]] की अभिक्रिया द्वारा उत्पन्न लवणों को नाइट्रेट कहते हैं। सामान्य ताप पर नाइट्रेट ठोस क्रिस्टल होते हैं। अधिकतर नाइट्रेट श्वेत रंग के पदार्थ हैं, परंतु कुछ जलीय नाइट्रेट (जैसे कोबाल्ट, निकेल, ताम्र नाइट्रेट) रंगीन भी होते हैं। गरम करने पर इनका विघटन हो जाता है। | |||
| | |||
सामान्यत: नाइट्रेट जल में विलेय होते हैं। अनेक नाइट्रेट वायुमंडल से जलवाष्प का अवशोषण कर लेते हैं। इन्हें आर्द्रताग्राही (hygroscopic) पदार्थ कहते हैं। गरम करने पर विघटन द्वारा नाइट्रेट की कुछ मात्रा ऑक्साइड में परिवर्तित हो जाती है और उससे नाइट्रिक अम्ल मुक्त होता है। | |||
क्षारीय विलयन में नाइट्रेट का ऐल्यूमिनियम अथवा जिंक द्वारा अपचयन हो जाता है। इस क्रिया का उपयोग नाइट्रेट के मात्रात्मक परिमापनों (quantitative measurements) में किया जाता है। | |||
== इन्हें भी देखें == | |||
* [[ऑक्सो-ऐनायन]] | |||
== सन्दर्भ == | |||
<small>{{reflist|2}}</small> | |||
[[श्रेणी:नाइट्रेट| *]] | |||
[[श्रेणी:ऑक्सो-ऐनायन]] | |||
[[श्रेणी:प्रकार्यात्मक समूह]] | |||
१८:५६, ५ अगस्त २०२० के समय का अवतरण
नाइट्रेट (nitrate) कार्बन [carbon] और नाइट्रोजन तत्वों [nitrogen] का बना एक ऋणायन (निगेटिव आवेश वाला आयन) होता है। इसका रासायनिक सूत्र NO3− है। यह अमोनियम नाइट्रेट जैसे कई रासायनिक यौगिकों (कम्पाउंड) का अंश है।[१]
धातुओं अथवा उनके ऑक्साइड पर नाइट्रिक अम्ल की अभिक्रिया द्वारा उत्पन्न लवणों को नाइट्रेट कहते हैं। सामान्य ताप पर नाइट्रेट ठोस क्रिस्टल होते हैं। अधिकतर नाइट्रेट श्वेत रंग के पदार्थ हैं, परंतु कुछ जलीय नाइट्रेट (जैसे कोबाल्ट, निकेल, ताम्र नाइट्रेट) रंगीन भी होते हैं। गरम करने पर इनका विघटन हो जाता है।
सामान्यत: नाइट्रेट जल में विलेय होते हैं। अनेक नाइट्रेट वायुमंडल से जलवाष्प का अवशोषण कर लेते हैं। इन्हें आर्द्रताग्राही (hygroscopic) पदार्थ कहते हैं। गरम करने पर विघटन द्वारा नाइट्रेट की कुछ मात्रा ऑक्साइड में परिवर्तित हो जाती है और उससे नाइट्रिक अम्ल मुक्त होता है।
क्षारीय विलयन में नाइट्रेट का ऐल्यूमिनियम अथवा जिंक द्वारा अपचयन हो जाता है। इस क्रिया का उपयोग नाइट्रेट के मात्रात्मक परिमापनों (quantitative measurements) में किया जाता है।
इन्हें भी देखें
सन्दर्भ
- ↑ Wolfgang Laue, Michael Thiemann, Erich Scheibler, Karl Wilhelm Wiegand "Nitrates and Nitrites" in Ullmann's Encyclopedia of Industrial Chemistry, 2006, Wiley-VCH, Weinheim. doi:10.1002/14356007.a17_265