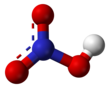
नाइट्रिक अम्ल
साँचा:Chembox Footer/tracking container onlyसाँचा:short description
नाइट्रिक अम्ल (Nitric acid) (<chem>HNO3</chem>), एक अत्यन्त संक्षारक (कोरोसिव) खनिज अम्ल है। इसे एक्वा फ्रोटिस (aqua fortis) और 'स्पिरिट ऑफ नाइटर' भी कहते हैं।
कीमियागरों को नाइट्रिक अम्ल का ज्ञान था, जिसे वे ऐक्वा फॉर्टिस के नाम से पुकारते थे। प्रसिद्ध कीमियागर जेबर ने नाइटर (niter) और ताम्र सल्फेट, (Cu SO4) तथा फिटकरी के साथ आसवन से प्राप्त कर इसका वर्णन किया है। भारत में शोरा तथा नाइट्रिक अम्ल का १६वीं शताब्दी में ज्ञान था। शुक्राचार्य के ग्रंथ शुक्रनीति में बारूद बनाने के लिए इसे उपयोग का वर्णन हुआ है। उड़ीसा के गजपति प्रतापरुद्रदेव द्वारा लिखित ग्रंथ 'कौतुकचिंतामणि' में यवक्षार (साल्टपीटर) का उल्लेख है। इसके अतिरिक्त सुवर्णतंत्र ग्रंथ (लगभग १७वीं शताब्दी में लिखा गया) में 'शंखद्राव' का वर्णन है, जो शोरे और नमक के अम्लों (HCl) का मिश्रण था। आईने अकबरी ग्रंथ में रासी (शोरे के अम्ल) का वर्णन है, जिसका चाँदी को स्वच्छ करने में उपयोग हो सकता था।
वर्ष १६४८ ई॰ में ग्लॉबर (Glauber) ने नाइटर पर विट्रियल तेल (oil of vitreol) की अभिक्रिया द्वारा संद्र नाइट्रिक अम्ल का निर्माण किया। कैवेंडिश ने १७७६ ई॰ में इसका संघटन ज्ञात किया। वायुमंडल में नाइट्रिक अम्ल विद्युत विसर्जन (electric discharge) द्वारा सूक्ष्म मात्रा में बनता रहता है, जो वर्षाजल में घुलकर पृथ्वी पर आता है। मिट्टी में उपस्थित कार्बनिक पदार्थों के ऑक्सीकरण द्वारा भी नाइट्रिक अम्ल बनता है। यह अम्ल अनेक नाइट्रेट पदार्थों के रूप में भूमि में संचित होकर पौधों के उपयोग में आता है। नाइट्रेट यौगिकों का प्रमुख स्रोत चिली देश है। भारत की साँभर झील में पोटाशियम नाइट्रेट पाया जाता है। भारत के कुछ राज्यों में मिट्टी के साथ मिला हुआ पोटासियम नाइट्रेट पाया जाता है। इससे एक समय प्रचुर मात्रा में शोरा (व्यापारिक पोटासियम नाइट्रेट) तैयार होता था।
निर्माण
प्रयोगशाला में अब भी नाइट्रिक अम्ल सोडियम (<chem>NaNO3</chem>), और सांद्र सल्फ्यूरिक अम्ल मिश्रण को गरम कर तैयार किया जाता है। उत्पन्न वाष्प अम्ल को एक ठंडे बरतन में निर्वात में जमा करते हैं। अभिक्रिया का समीकरण निम्नलिखित है:
<chem>NaNO3 + H2SO4 -> NaHSO4 + HNO3</chem>
पूर्वकाल में व्यापारिक मात्रा में इसी अभिक्रिया द्वारा नाइट्रिक अम्ल तैयार किया जाता था।
दूसरी क्रिया के अनुसार वायुमंडल के ऑक्सीजन तथा नाइट्रोजन को विद्युत विसर्जन द्वारा संयुक्त कर नाइट्रिक अम्ल बनाते हैं। यह अभिक्रिया बर्कलैंड तथा आइड प्रक्रिया (Birkland and Eyde process) कहलाती है। विद्युत् का अत्यधिक व्यय और अम्ल की न्यून प्राप्ति के कारण इस प्रक्रिया को अब काम में नहीं लाते।
सामान्यत: नाइट्रिक अम्ल का उत्पादन अमोनिया (<chem>NH3</chem>), के उत्प्रेरकीय ऑक्सीकरण द्वारा होता है। अमोनिया और वायु के सम्मिश्रण को ६०० डिग्री सेल्सियस तक गरम कर, प्लेटिनम धातु की जाली में होकर प्रवाहित करने पर, अमोनिया का ऑक्सीकरण हो जाता है :
<chem>4NH3 + 5O2 -> 4NO + 6H2O + 215,000 Cal.</chem>
यह अभिक्रिया ऊष्माक्षेपी (exothermic) है और इसमें सम्मिश्रण १,००० डिग्री सेल्सियस तक गरम हो जाता है। तत्पश्चात् गैसों को निम्न ताप पर लाने से नाइट्रिक ऑक्साइड तथा ऑक्सीजन के बीच अभिक्रिया होती है :
<chem>2NO + O2 -> 2NO2 + 27,800 Cal</chem>
उत्पन्न नाइट्रिक द्विऑक्साइड को ठंडा कर अवशोषण स्तंभ (absorption towers) द्वारा प्रवाहित करते हैं, जिसमें जल की बौछार गिरती है। यहाँ पर नाइट्रिक अम्ल बनता है :
<chem>3NO2 + H2O -> 2HNO3 + NO</chem>
बचे नाइट्रिक ऑक्साइड को फिर से प्रवाहित किया जाता है।
गुण
विशुद्ध नाइट्रिक अम्ल रंगहीन द्रव है, इसका अणुभार ६३, गलनांक - ४२ डिग्री सेल्सियस्, क्वथनांक ८६ डिग्री सेल्सियस् तथा घनत्व १.५२ ग्राम प्रति घन सेंमी॰ है। नाइट्रिक अम्ल सशक्त अम्ल है और जलीय विलयन में पूर्णत: हाइड्रोजन आयन (H+) एवं नाइट्रेट आयन (NO-3) में विघटित हो जाता है। इसके ६८ प्रतिशत जल मिश्रण का क्वथनांक १२०.५ डिग्री सेल्सियस है। इसे 'नियत क्वथनांक मिश्रण' (constant boiling mixture) कहते हैं। नाइट्रिक अम्ल सामान्य ताप पर धीरे-धीरे विघटित होता रहता है। उच्च ताप पर अथवा तीव्र प्रकाश में इसकी विघटन गति बढ़ जाती है।
नाइट्रिक अम्ल में ऑक्सीकारक गुण प्रधान हैं। कुछ उत्कृष्ट धातुओं (स्वर्ण, प्लेटिनम, इरीडियम, रोडियम तथा टैंटेलम) को छोड़कर प्रत्येक धातु को यह आक्रांत करता है। यह बहुधा धातुओं तथा अधातुओं का ऑक्सीकरण कर नाइट्रोजन के ऑक्साइड, नाइट्रोन, हाइड्राविसलएैमीन (<chem>NH2OH</chem>), अथवा अमोनिया मुक्त करता है। लौह, ताँबा अथवा क्रोमियम, सांद्र नाईटिक अम्ल के संपर्क से निष्क्रिय (passive) हो जाते हैं। तत्पश्चात् उनकी रासायनिक अभिक्रिया बहुत क्षीण हो जाती है। ऐसा अनुमान है कि यह परिवर्तन उपर्युक्त धातुओं की सतह पर ऑक्साइड की परत जम जाने के कारण आ जाता है। यदि उनपर जमी परत को खुरच दिया जाए तो वे फिर सक्रिय हो जाते हैं।
उपयोग
नाइट्रिक अम्ल का उपयोग रासायनिक उद्योगों में बहुत मात्रा में हो रहा है। इसके अम्लीय तथा ऑक्सीकारक गुणों के कारण यह अनेक कार्बनिक तथा अकार्बनिक अभिक्रियाओं में काम आता है। इसका विशेष उपयोग विस्फोटक पदार्थ, रंजकों (dyes) तथा दवाइयों के बनाने में हुआ है। इसके लवण एवं अन्य यौगिक उर्वरक के रूप में काम आते हैं।